验证血浆淀粉样蛋白β42/40用于检测阿尔茨海默病淀粉样蛋白斑块
Validation of Plasma Amyloid-β 42/40 for Detecting Alzheimer Disease Amyloid Plaques
验证血浆淀粉样蛋白β42/40用于检测阿尔茨海默病淀粉样蛋白斑块
摘要译文
目的:采用多个中心利用不同的血液采集和处理方案采集的样本,确定血浆Aβ42/Aβ40检测在全球研究中对区分淀粉样蛋白PET状态的准确性。
方法:从美国(n=182)、澳大利亚(n=183)和瑞典(n=100)的3个大型阿尔茨海默病(AD)研究队列获取血浆样本(n=465)。采用高精度免疫沉淀质谱(IPMS)测定法,测定血浆Aβ42/Aβ40,并与淀粉样蛋白PET及CSF Aβ42/Aβ40的参照标准比较。
结果:在包括465例受试者的综合队列中,血浆Aβ42/Aβ40与淀粉样蛋白PET水平有良好的一致性(受试者操作特征曲线下面积[AUC]为0.84,95%置信区间[CI]0.80 - 0.87);纳入APOE ε4水平后,一致性改善(AUC 0.88,95% CI 0.85-0.91)。血浆Aβ42/Aβ40与CSF淀粉样蛋白水平的AUC为0.85(95% CI 0.78-0.91),加入APOE ε4水平后,改善为0.93(95% CI 0.89-0.97)。在三个队列中,尽管方案有差异,但这些发现都一致。而且,这种检测法在认知未受损和受损个体中的性能相似。
结论:血浆Aβ42/Aβ40是检测淀粉样蛋白斑块的稳健指标,有助于AD的诊断,可用于识别有可能因AD导致未来痴呆的个体,改善入组AD研究和临床试验的人群的多样性。
证据分类:这项研究提供了II类证据,证明通过高精度IPMS测定法测定的血浆Aβ42/Aβ40在认知未受损和受损的研究受试者中均可准确诊断脑淀粉样变。
原文链接:
https://n.neurology.org/content/98/7/e688.long
Li Y, Schindler SE, Bollinger JG,et al.Neurology. 2022 Feb 15;98(7):e688-e699.
解读人:胡晓琴
宜昌市第一人民医院神经内科副主任医师
宜昌市神经病学分会委员,精神医学分会委员

研究解读
2022年2月,美国华盛顿大学神经病学系的Randall J. Bateman 在Neurology上发表了题为“Validation of Plasma Amyloid-β 42/40 for Detecting Alzheimer Disease Amyloid Plaques”(《验证血浆β淀粉样蛋白42/40用于检测阿尔茨海默病淀粉样蛋白斑块》)的文章,发现血浆Aβ42/Aβ40与脑脊液Aβ42/Aβ40之间的相关性很强。
阿尔茨海默病(AD)的大脑病理,其特征是淀粉样斑块和神经纤维缠结,在大多数人出现痴呆症状之前,在大脑中积累了10到20年。在认知功能未受损的个体中,AD的生物标记物用于识别AD痴呆风险人群,以纳入旨在延缓或者预防AD痴呆症状发展的临床实验。在认知功能受损的个体中,AD的生物标志物被用来评估AD是否是痴呆症状的潜在原因。随着AD修饰药物的研发,如何准确的找出大脑内有淀粉样斑块沉积的病人成为了主要挑战。
研究发现,血浆Aβ42/Aβ40出现异常早于AβPET。用ELISA等传统技术测量血浆Aβ42,Aβ40有比较大的偏差,在区分淀粉样蛋白阳性和阴性个体时表现较差。基于质谱分析检测的血浆Aβ42/Aβ40是优于其他检测方法的。最近的研究比较了不同质谱和免疫学检测的性能,发现IPMS检测血浆Aβ42/Aβ40与淀粉样蛋白PET状态的一致性最高。采用IPMS检测血浆aβ42/ aβ40作为脑淀粉样变的生物标志物的准确性需要在多个队列中进行验证,以确立其准确性和稳定性。目前尚不清楚血浆Aβ42/Aβ40是否可以在不同中心和队列中使用不同的收集方法进行一致的测定。同样,也不清楚血浆a β42/ a β40是否对认知功能未受损和受损的人都是一种可靠的脑淀粉样变测量方法。
研究在美国,欧洲和澳大利亚三个不同的AD研究中心采用IPMS法检测血浆aβ42/ aβ40。在三个研究中,采集认知功能受损和认知功能正常的人群血液,通过不同的血液收集和处理流程来检测血浆内a β42/ a β40,从而了解血浆a β42/ a β40是否可以准确的检测出脑内淀粉样蛋白的沉积。
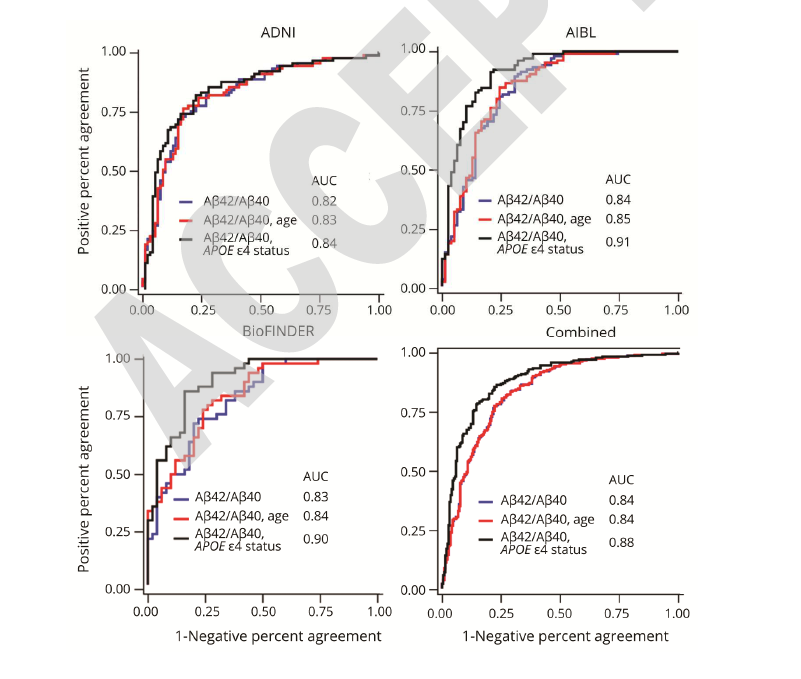
该测试通常在非禁食条件下抽取血液,较适用于常规临床环境。不同队列和研究之间的相似临界值明,血浆Aβ42/Aβ40检测在使用不同抗凝剂和离心条件的血液采集和处理方案中是一致的。实验表明,在三个独立的队列中,使用不同的采血和处理方案,以及多种不同的淀粉样蛋白示踪剂,血浆a β42/ a β40和淀粉样蛋白PET之间有良好的一致性。在BioFINDER队列中测试一致性最佳。在每个单队列中以及联合队列中,与淀粉样PET阴性组相比,淀粉样PET阳性组血浆Aβ42/Aβ40较低(p<0.0001)。ROC分析显示,血浆Aβ42/Aβ40单队列预测淀粉样PET水平的AUC范围为ADNI 0.82至AIBL 0.84;而联合队列的AUC为0.84 (95% CI 0.80-0.87)。根据Youden指数,区分淀粉样PET水平的最佳血浆Aβ42/Aβ40临界值在三个队列中是相似,从AIBL和BioFINDER的0.123到ADNI的0.125。在联合队列中,临界值为0.123与淀粉样PET水平的阳性符合率(PPA)为0.77,阴性符合率(NPA)为0.78,与淀粉样PET水平一致的准确率为0.80。
此外,本研究还发现,与淀粉样PET阴性个体相比,淀粉样PET阳性受试者年龄较大(73.7 6.8 vs 72.0 7.2, p = 0.01),更有可能携带APOE ε4等位基因(64% vs 20%, p<0.0001),认知功能受损的可能性更大(59%比48%,p = 0.01)。三个队列中,与单独血浆Aβ42/Aβ40相比,血浆Aβ42/Aβ40联合APOE ε4状态提高了预测淀粉样PET状态的能力,并且血浆Aβ42/Aβ40联合APOE ε4检测既能在认知功能受损个体也能在未受损的个体中区分淀粉样PET的状态。这些结果表明,血浆Aβ42/Aβ40联合APOE ε4状态有助于筛查认无知障碍的个体参加AD二级预防临床试验,也有助于在临床中检测认知障碍个体以确定AD是否是可能的病因。
在本研究中,淀粉样PET状态和脑脊液Aβ42/Aβ40状态是根据各研究提供的临界值定义的。为了说明队列之间潜在的方法学差异,在联合队列分析中,我们使用了混合效应模型,并对每个队列进行随机截取。观察到血浆Aβ42/Aβ40,淀粉样蛋白PET和脑脊液Aβ42/Aβ40之间的相关性与其他研究报道相似。虽然它们相关性很强,但是比值并不接近1,说明这三种测量方法提供的信息不完全相同(图1)。血浆Aβ42/Aβ40、脑脊液Aβ42/Aβ40与淀粉样PET之间的差异及随时间的关系有待进一步研究。
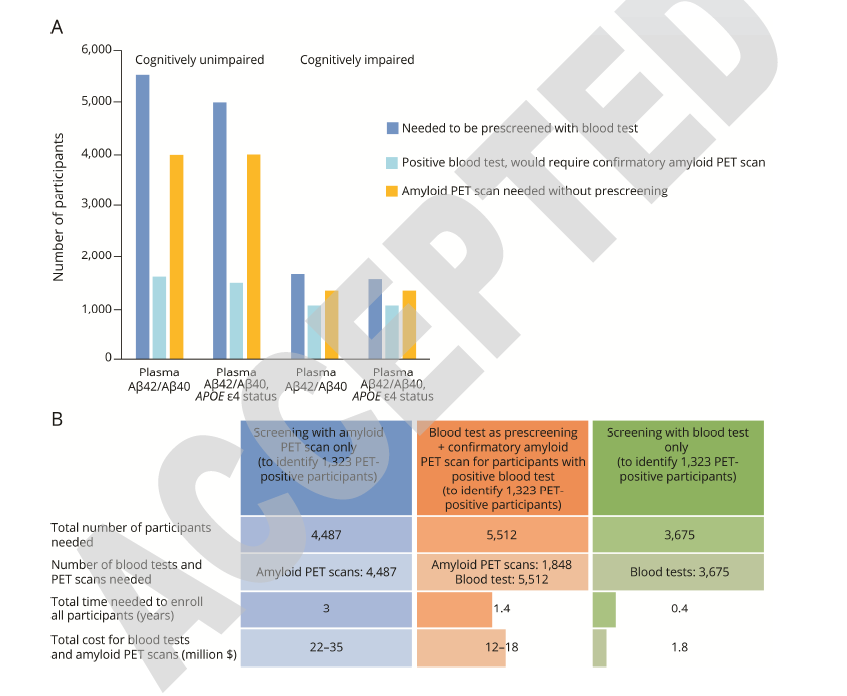
本研究还评估了筛选1000例淀粉样PET阳性受试者所需要的参与PET扫描的人数(参与者预先做或不做血液检测均可)。对于认知功能未受损的个体,预先进行血液检测可减少所需淀粉样PET扫描次数59%(仅血浆Aβ42/ Aβ40进行筛查)或62%(血浆Aβ42/ Aβ40和APOE ε4状态进行筛查)(图2)。对于认知功能受损的个体,预先进行血液检测筛查可以减少大约19%的淀粉样PET扫描。在一项类似于无症状阿尔茨海默病抗淀粉样蛋白治疗研究的AD预防试验中,评估了用血液检测对脑淀粉样变进行前期筛查所节省的时间和成本。血液检测预筛查减少了一半的登记时间和筛查费用。这些数据表明,当淀粉样PET阳性率在人群中较低时(例如,认知功能未受损的人群),血液测试的预筛查更有效,具有高灵敏度和特异性的检测方法在减少被筛查参与者的数量和需要的验证性PET扫描的数量方面效率更高。
(表据American Academy of Neurology)
图1区分淀粉样PET状态的受试者工作特征曲线
蓝色=血浆Aβ42/Aβ40;红色=血浆Aβ42/Aβ40及年龄;黑色=血浆Aβ42/Aβ40和APOE ε4状态。
(表据American Academy of Neurology)
图2血浆a β42/ a β40作为脑淀粉样变的预筛选试验。(A)参与者的数量和淀粉样PET扫描需要确定1000个淀粉样PET阳性参与者,无论有没有血液测试的预筛选。认知功能未受损组淀粉样PET阳性率为25%,认知功能受损组为75%。血浆Aβ42/40检测的敏感性和特异性采用表6提供的数据。(B)血浆Aβ42/Aβ40预筛查脑淀粉样变所节省的时间和成本被评估用于一项AD预防试验,类似于无症状阿尔茨海默病抗淀粉样蛋白治疗研究(A4)。在A4研究中,4487名参与者在三年的时间里进行了淀粉样PET扫描,其中1323名参与者(30%)被归类为淀粉样PET阳性。根据表6所示认知正常受试者的敏感性为0.80,特异性为0.83,检测血液检测的准确性。成本假设为每次淀粉样PET扫描5000 - 8000美元,每次血液检查500美元。