遗忘型轻度认知障碍和阿尔茨海默病中肠道微生物代谢物的改变:宿主-微生物相互作用中的信号
摘要译文
宿主-微生物的代谢互动调节健康和疾病状态下的免疫、代谢和神经元反应,但尚未用于疾病的生物标志物或干预。我们最近的研究发现遗忘型轻度认知障碍(aMCI)和阿尔茨海默病(AD)痴呆患者的微生物组发生了改变。因此,我们旨在确定AD、aMCI和健康对照(HC)肠道微生物代谢产物的特征。本研究招募了77例被试(22例aMCI、27例AD和28例HC),通过液相色谱/气相色谱-质谱代谢组学分析,我们发现AD和HC在色氨酸代谢物、短链脂肪酸(SCFAs)和石胆酸方面存在显著差异,其中大多数代谢变化与微生物群改变和认知损害相关。aMCI出现色氨酸紊乱,SCFAs从aMCI到AD逐渐减少。色氨酸的代谢物吲哚-3-丙酮酸被确定为是鉴别和预测AD的标志物,五种SCFAs被确定为AD发病前和进展期的标志物。该研究结果表明,基于粪便的肠道微生物特征与AD的发生发展相关;这为AD预防中的微生物群或饮食干预提供了一个潜在的靶点,并支持AD病理生理学中的宿主-微生物信号互动理论。
关键词:阿尔茨海默病;粪便代谢组学;肠道菌群;色氨酸;短链脂肪酸
原文链接:
https://www.mdpi.com/2072-6643/13/1/228
Wu L, Han Y, Zheng Z, et al. Nutrients. 2021;13(1):228.

解读人:葛宇松 教授
l 大连医科大学附属第二医院神经内二科副主任,教授,主任医师,硕士生导师,学科建设与科研管理部主任
l 中华医学会肠外肠内营养学分会“脑健康营养协作组”组员、中国卒中学会脑健康分会第一届青年委员会委员、辽宁省基层卫生协会脑血管病专业委员会常委、辽宁省细胞生物学学会老年痴呆与认知障碍专业委员
研究解读
2021年1月浙江大学医学院附属第一医院王保红教授课题组在Nutrients上发表了一篇题为“Altered Gut Microbial Metabolites in Amnestic Mild Cognitive Impairment and Alzheimer's Disease: Signals in Host-Microbe Interplay”(《遗忘型轻度认知障碍和阿尔茨海默病中肠道微生物代谢物的改变:宿主-微生物相互作用中的信号》)的研究论文。该研究应用高分辨率的非靶向和靶向粪便代谢组学研究,以分析和量化中国队列中的遗忘型轻度认知障碍(aMCI)、早期阿尔茨海默病(AD)患者和正常认知健康对照(HC)的微生物特征。将AD的粪便代谢物差异与肠道菌群失调和认知障碍相关联,由此发现与AD相关的潜在微生物生物标志物,可用于改善AD的早期检测,开辟治疗机会。
本研究招募了77例受试者(22例aMCI、27例AD、28例HC)。所有受试者均接受完整的病史评价、体格检查、神经、神经心理学评估(简易精神状态检查量表[MMSE]和北京版蒙特利尔认知评估量表[MoCA])、神经影像学检查(磁共振成像)和临床生化检查。通过临床痴呆评定量表(CDR)评价衰老性痴呆的严重程度。在基线访视时采集早晨空腹血清和粪便样本。所有研究对象均进行粪便非靶向代谢组学分析和多变量数据分析,并对粪便进行色氨酸、短链脂肪酸(SCFAs)及胆汁酸(BA)的靶向分析,同时进行血清脂多糖(LPS)水平测定。
粪便代谢物代谢组学研究发现,与HC受试者相比,发病前aMCI和AD具有独特的粪便代谢组学。在AD患者中发现色氨酸、SCFAs和BA等三类代谢物的变化,这些变化与肠道微生态失调和认知障碍有关。
人们普遍认为色氨酸可作为协调胃肠道生理学和中枢神经系统功能的关键先决条件,通过调节吲哚衍生物、犬尿氨酸途径和5-羟色胺(5-HT)合成实现。此研究发现AD的粪便代谢组学以色氨酸代谢的显著变化为特征,尤其是吲哚衍生物和5-HT合成,并且研究揭示了粪便吲哚-3-丙酮酸(IPYA)在发病前aMCI和AD中富集,这与肠道微生态失调和AD发展显著相关。粪便IPYA可以将AD和aMCI与正常认知HC进行区分,可能是肠道微生态失调的介质并参与AD的发展,因此是从治疗角度预防或治疗AD的潜在靶点。
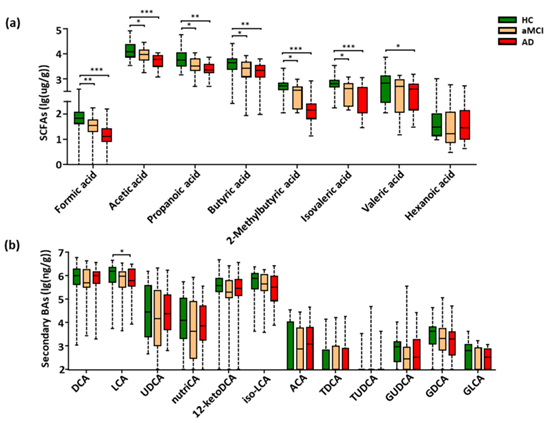
在所有受试者的粪便中共检测到8种SCFAs。与HC相比,7种SCFAs从aMCI至AD呈进行性下降趋势,其中6种在aMCI和AD中均显著降低,戊酸在AD中显著降低(图1a)。5种SCFAs(甲酸、乙酸、丙酸、2-甲基丁酸和异戊酸)显示aMCI和AD患者之间存在显著差异。总之,这些结果表明粪便SCFAs的变化与AD的疾病进展相关,SCFAs对从aMCI转化为AD具有很强的预测能力。
在所有受试者中共检测到18种原发性和继发性BAs。与HC相比,仅细胞毒性石胆酸(LCA)显示从HC至aMCI和AD的趋势逐渐降低,AD显著降低(图1b),此研究结果为肠源性胆汁酸LCA在AD发病机制中的作用增加了新的线索。
鉴于促炎LPS在认知障碍中的作用,研究测定了循环LPS水平。与HC相比,发病前aMCI和AD患者的血清LPS有增加趋势。
研究者们假设,与AD患者相关的肠道微生态失调导致色氨酸、SCFAs和BAs的代谢失调,肠道微生物-代谢产物的变化可增加肠道通透性,允许LPS转移,或直接引发或加重神经炎症和神经传递障碍,最终促进AD进展。
此研究仍存在一定的局限性。例如,招募的志愿者拒绝进行腰椎穿刺进行脑脊液(CSF)测定和正电子发射断层扫描成像,因此缺少生物标志物的确诊。其次,这项观察性研究未能证明微生物代谢物在AD发生中的因果关系。然而,这些代谢物中的大多数随着疾病进展而逐渐改变,并与认知障碍显著相关,强烈表明其在AD中的关键作用。这需要在大型队列纵向研究中进一步确定其因果关系。
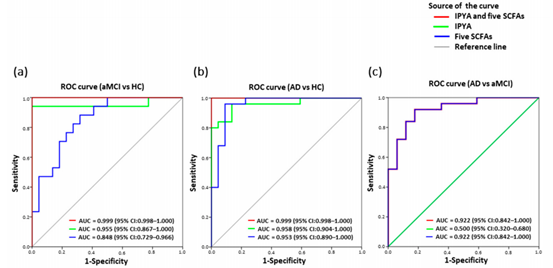
总之,此研究通过分析发病前aMCI和AD的粪便代谢组学,揭示了AD粪便微生物特征的改变。粪便微生物群-代谢组学的变化指出色氨酸、SCFAs和BAs的失调通路。有趣的是,粪便IPYA首次被报道可将发病前aMCI和AD与HC进行区分,5种SCFAs可区分AD与aMCI。重要的是,当IPYA结合5种SCFAs测量时,检测AD和aMCI的效果最好(图2)。因此,这些发现提供了粪便微生物特征可能是AD筛查和管理的非侵入性生物标志物的证据,靶向肠道菌群或微生物代谢可能是预防和治疗AD的一种有前景的方法。
(图据Nutrients)
图1. 从HC到aMCI和AD患者,SCFAs和LCA水平逐渐降低。(a,b) HC、aMCI和AD组粪便SCFAs和粪便次级胆汁酸的比较。注:数据表示为中位数和范围,使用单因素ANOVA或Kruskal–Wallis检验计算P值。*P<0.05;**P<0.01;***P<0.001。缩略语:SCFAs,短链脂肪酸;DCA,脱氧胆酸;LCA,石胆酸;UDCA,熊去氧胆酸;nutriCA,营养胆酸;12-ketoDCA,12-酮脱氧胆酸;iso-LCA,异石胆酸;ACA,别胆酸;TDCA,牛磺脱氧胆酸;TUDCA,牛磺熊去氧胆酸;GUDCA,甘氨酰脱氧胆酸;GDCA,甘氨脱氧胆酸;GLCA,葡糖石胆酸;BA,胆汁酸;ANOVA,方差分析。
(图据Nutrients)
图2. 使用6种粪便微生物代谢物组合的AD患者分类和预测。通过进行二元多变量逻辑回归分析,建立基于色氨酸代谢物IPYA和5种SCFAs(甲酸、乙酸、丙酸、2-甲基丁酸和异戊酸)的预测模型。计算区分(a)aMCI与HC、(b)AD与HC、(c)AD与aMCI的ROC曲线。缩略语:ROC,受试者工作特征;AUC,ROC曲线下面积;CI,置信区间。