Brief introduction: The Brain-Gut-Microbiome Axis
节选译文
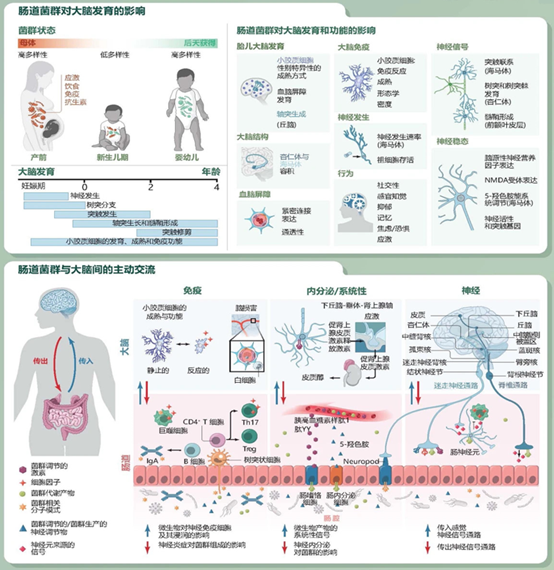
肠道微生物群对大脑发育的影响
肠道微生物群从生命的最初阶段就开始影响宿主的生理特性。肠道微生物群的改变可能不利于器官系统(包括大脑)发育的关键过程。对无菌饲养、使用抗生素治疗或受环境因素影响而改变的母体或产后早期微生物群的动物研究显示,通过调节神经元的产生、特异性和成熟,可以导致大脑免疫、血脑屏障通透性、大脑结构和神经回路出现异常。这些影响可以持续到成年,并导致长期行为缺陷,这强调了良好平衡的微生物群对于关键的神经发育窗口期的重要性。尽管微生物组影响胎儿稳态的证据正在快速出现,但仍需进一步的研究来揭示肠道微生物调节早期大脑发育和成熟的精确机制。
肠道微生物组与大脑之间的主动交流
肠道微生物组与中枢神经系统(CNS)之间的主动交流可以通过至少三个平行和互连的途径实现。
原文链接:
https://www.cell.com/cell/retrieve/pii/S0092867421003500?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867421003500%3Fshowall%3Dtrue
Agirman G, Hsiao EY.Cell.2021. Cell. 2021;184(9):2524-2524.e1.
解读人:吴钢教授 福建三博福能脑科医院神经内科主任医师
文献解读
2021年4月,加州大学洛杉矶分校综合生物与生理学系的Gulistan Agirman和Elaine Y. Hsiao在国际知名期刊Cell(《细胞》)上发表了题为《简要介绍:微生物-肠-脑轴》的文章。该文章通过图文结合的形式非常生动地诠释了肠道微生物对大脑发育和功能的影响,以及微生物-肠-脑轴是如何实现相互作用的。
微生物-肠-脑轴的机制尚未完全研究清楚,但肠道微生物对大脑的影响其实从生命早期阶段就开始了。在婴儿大脑不断发育的同时,肠道微生物组也在经历变化,在出生前的母体内是一个高多样性的状态,婴儿出生后处于低多样性的状态,而随着婴儿的成长,又会趋于高多样性的状态。文中指出,对无菌饲养、抗生素治疗或受环境因素影响而改变母体或产后早期微生物组的动物研究显示,通过调节神经元的产生、特异性和成熟,可以导致大脑免疫、血脑屏障通透性、大脑结构和神经回路出现异常。而这些影响不是暂时的,甚至可以持续至成年,因此维持肠道菌群的平衡对维持大脑发育和功能的正常非常重要。
从肠道到大脑,距离如此遥远的器官如何实现联系仍是值得不断探索的课题。在该文中,作者总结了3条平行和互连的通路。
第一条通路是免疫途径。肠道微生物可以通过影响外周和中枢的免疫细胞对大脑产生影响,在神经炎性疾病的背景下,血脑屏障通透性的改变可以促进微生物产物的通过和外周免疫细胞对脑实质的侵袭。而起源于大脑以应对卒中等疾病的炎症可以改变肠道微生物组,从而导致恶性循环,肠道菌群失调会加剧神经免疫反应并加重大脑病理和行为。
第二条通路是内分泌/系统途径。这一途径的实现依赖于微生物产物和代谢物对相关信号的激活。据报道,肠道微生物群与下丘脑-垂体-肾上腺(HPA)轴介导的神经内分泌信号通路存在双向作用。压力诱导的HPA轴激活会影响胃肠功能,并随后改变肠道微生物组的组成。相反,肠道微生物群的消耗会改变HPA轴的功能。
第三条通路是神经元途径。微生物产物的子集、微生物群调节的激素和微生物群依赖的免疫介质可以直接与内在的肠神经元、肠道支配的迷走神经和脊髓传入相互作用。然后局部信号通过感觉回路传递到涉及认知、情绪、恐惧/焦虑、躯体感觉和/或进食行为的大脑区域。反过来,迷走神经和脊髓传出神经投射到肠粘膜并直接影响胃肠道稳态或通过与肠神经系统的相互作用间接影响胃肠道稳态。
文章同时也指出构成微生物-肠-脑轴的免疫、内分泌/系统和神经元通路高度复杂且相互关联。例如,刺激肠道常驻免疫细胞可导致炎症细胞因子的局部和全身释放,并影响肠道和大脑的通透性,这有利于微生物副产物进入门静脉循环和肠实质,调节局部神经末梢的兴奋性,最终改变大脑稳态。肠道内分泌和神经系统之间也可产生直接作用,肠内分泌细胞的神经足可与传入迷走神经纤维接触并起到兴奋性突触的作用,从而直接快速地将微生物相关信号传递到大脑。
该文章为我们展示了微生物-肠-脑轴涉及跨器官系统的复杂相互作用,而这些相互作用是通过多种途径和在不同的时间维度发生的。随着研究的不断进行,健康状态和疾病状态中微生物-肠-脑轴信号传递的基本原理和精确机制将被进一步阐明。
(编译自cell)